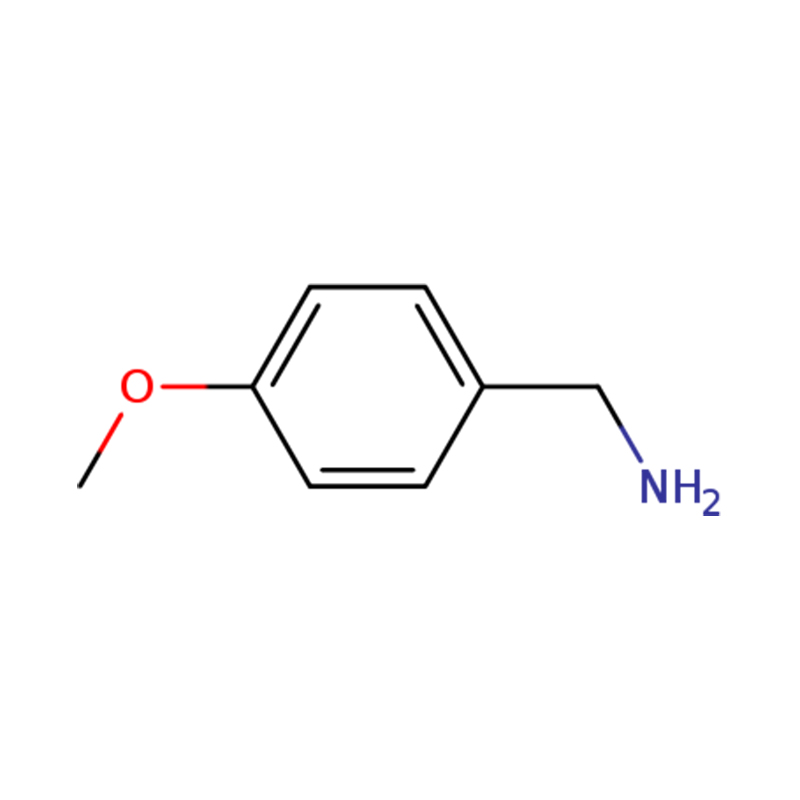
1-(4-METOXIFENIL)METANAMINA
Detalhes do produto
| CasNo | 2393-23-9 | Prazo de entrega | dentro de 10 dias |
| Molecular | C8H11NO | Capacidade de produção | 1 tonelada métrica/dia |
| Aparência | Líquido transparente, incolor a ligeiramente amarelado | Pureza | 99%mínimo |
| Aplicativo | Intermediários farmacêuticos | Armazenar | Temperatura ambiente, escuro, lacrado |
| LimitNum | 1 quilograma | Transporte | Ar, mar, expresso. |
| Densidade | 1,05g/mLat25°C(lit.) | Ponto de ebulição | 236-237°C (lit.) |
| Ponto de Fusão | -10°C | Índice de refração | n20/D1.546(lit.) |
| Ponto de inflamação: | >230°F | Solubilidade | Altamente solúvel em água. |
| Nome | p-anisilamina ou (4-metoxifenil)metanamina |
Sinônimos
LABOTEST-BB LTBB000703; AKOS BBS-00003589; 4-AMINOMETIL-ANISOL; 4-METOXIBENZILAMINA; Cloridrato de P-Metoxibenzilamina 173,64; 4-Metoxibenzilamina, 98+%; para Esparfloxacina; CLORIDRATO DE P-METOXIBENZILAMINA
Aplicativo
Pode ser utilizado na síntese de intermediários farmacêuticos. É ligeiramente nocivo à água. Não permita que o produto, em sua forma pura ou em grandes quantidades, entre em contato com águas subterrâneas, cursos d'água ou sistemas de esgoto. Sem autorização governamental, não descarte o material no meio ambiente para evitar a formação de óxidos, ácidos, ar ou dióxido de carbono. Mantenha o recipiente bem fechado, em local hermeticamente fechado e armazenado em local fresco e seco.
Laboratório de Controle de Qualidade
Um laboratório de controle de qualidade individual está localizado nas instalações, onde são realizados testes químicos, físicos, microbiológicos, estudos de estabilidade e testes instrumentais, como IR, UV, HPLC e GC, para matérias-primas e produtos acabados. Toda a área possui acesso controlado e é bem conservada, com instrumentos analíticos suficientes para os testes realizados. Todos os instrumentos estão devidamente identificados e calibrados.
QA
A Garantia da Qualidade (QA) é responsável por avaliar e categorizar os desvios em nível Grave, Geral e Leve. Para todos os níveis de desvio, é necessária uma investigação para identificar a causa raiz ou a causa potencial. A investigação deve ser concluída em até 7 dias úteis. A avaliação do impacto no produto, juntamente com o plano de Ação Corretiva e Preventiva (CAPA), também é necessária após a conclusão da investigação e a identificação da causa raiz. O desvio é considerado encerrado quando o CAPA é implementado. Todos os desvios, independentemente do nível, devem ser aprovados pelo Gerente de QA. Após a implementação, a eficácia do CAPA é confirmada com base no plano.