Já em 24 de agosto de 2021, a Cara Therapeutics e sua parceira Vifor Pharma anunciaram que seu agonista do receptor opioide kappa, o primeiro da sua classe, o difelikefalin (KORSUVA™), foi aprovado pelo FDA para o tratamento de pacientes com doença renal crônica (DRC) (prurido moderado/grave com tratamento de hemodiálise), com previsão de lançamento no primeiro trimestre de 2022. A Cara e a Vifor assinaram um acordo de licenciamento exclusivo para a comercialização do KORSUVA™ nos Estados Unidos e concordaram em vendê-lo para a Fresenius Medical. Dessa forma, a Cara e a Vifor detêm, cada uma, 60% e 40% da receita de vendas, excluindo a Fresenius Medical, respectivamente; cada uma delas detém 50% da receita de vendas da Fresenius Medical.
A prurido associada à DRC (DRC-aP) é uma prurido generalizada que ocorre com alta frequência e intensidade em pacientes com DRC submetidos à diálise. A prurido ocorre em cerca de 60% a 70% dos pacientes em diálise, dos quais 30% a 40% apresentam prurido moderado/grave, o que afeta seriamente a qualidade de vida (por exemplo, má qualidade do sono) e está associado à depressão. Não havia tratamento eficaz para a prurido relacionada à DRC até então, e a aprovação da difelikefalina ajuda a suprir essa grande lacuna no tratamento. Essa aprovação se baseia em dois estudos clínicos pivotais de Fase III apresentados no pedido de registro do medicamento: dados positivos dos estudos KALM-1 e KALM-2 nos EUA e globalmente, e dados de suporte de 32 estudos clínicos adicionais, que demonstram a boa tolerabilidade do KORSUVA™.
Recentemente, recebemos boas notícias do estudo clínico da difelikefalina no Japão: em 10/01/2022, a Cara anunciou que seus parceiros Maruishi Pharma e Kissey Pharma confirmaram o uso da injeção de difelikefalina no Japão para o tratamento da coceira em pacientes em hemodiálise. O objetivo primário dos ensaios clínicos de Fase III foi alcançado. Cento e setenta e oito pacientes receberam difelikefalina ou placebo por 6 semanas e participaram de um estudo de extensão aberto de 52 semanas. O objetivo primário (alteração na pontuação da escala numérica de avaliação da coceira) e o objetivo secundário (alteração na pontuação da coceira na Escala de Gravidade de Shiratori) apresentaram melhora significativa em relação ao valor basal no grupo da difelikefalina em comparação com o grupo placebo, sendo ambos bem tolerados.
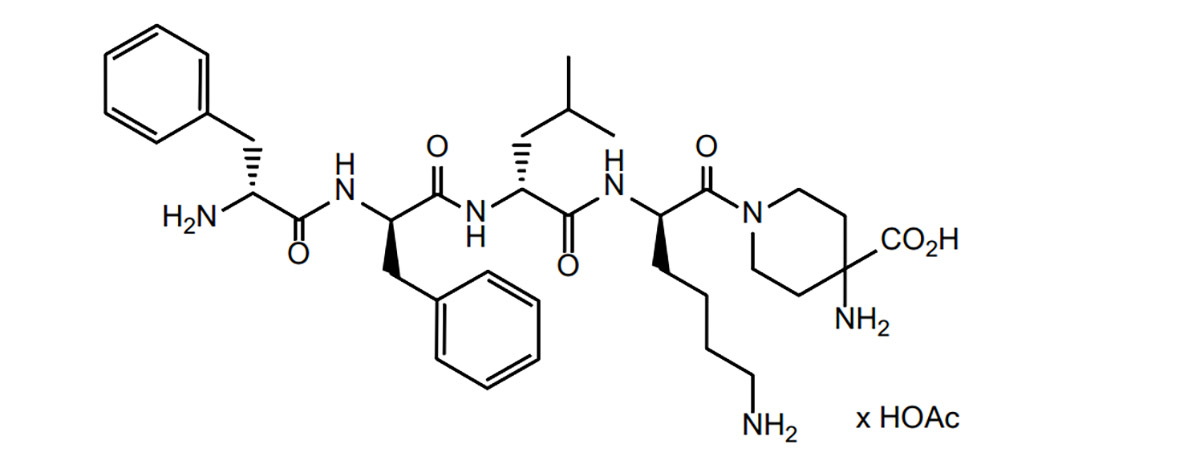
A difelikefalina é uma classe de peptídeos opioides. Com base nisso, o Instituto de Pesquisa de Peptídeos estudou a literatura sobre peptídeos opioides e resumiu as dificuldades e estratégias de desenvolvimento de fármacos com peptídeos opioides, bem como o panorama atual desse tema.
Data da publicação: 17 de fevereiro de 2022